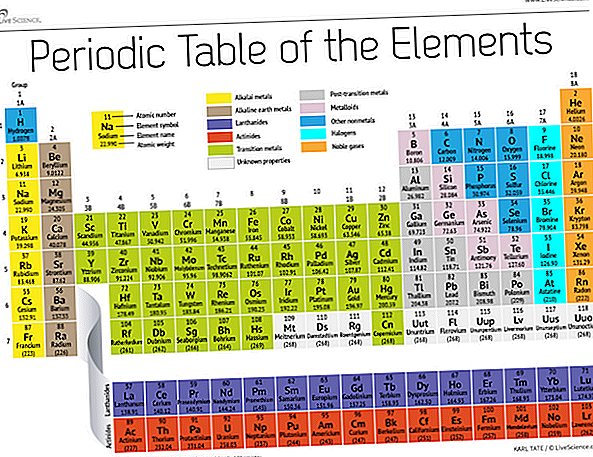
В края на 19 век руският химик Дмитрий Менделеев публикува първия си опит за групиране на химични елементи според атомните им тегла. По това време са били известни само около 60 елемента, но Менделеев осъзнава, че когато елементите се организират по тегло, определени видове елементи се появяват през равни интервали или периоди.
Днес, 150 години по-късно, химиците официално разпознават 118 елемента (след добавянето на четирима новодошли през 2016 г.) и все още използват периодичната таблица с елементи на Менделеев, за да ги организират. Таблицата започва с най-простия атом, водород и след това организира останалите елементи по атомно число, което е броят на протоните, които всеки съдържа. С шепа изключения редът на елементите съответства на нарастващата маса на всеки атом.
Таблицата има седем реда и 18 колони. Всеки ред представлява един период; числото на елемента на елемента показва колко от неговите енергийни нива притежават електрони. Натрият, например, седи в третия период, което означава, че натриевият атом обикновено има електрони в първите три енергийни нива. Придвижвайки се надолу по таблицата, периодите са по-дълги, защото са необходими повече електрони, за да се изпълнят по-големите и сложни външни нива.
Колоните на таблицата представляват групи или групи от елементи. Елементите в група често изглеждат и се държат по подобен начин, защото имат еднакъв брой електрони в най-външната си обвивка - лицето, което показват на света. Елементите от група 18 в най-дясната част на масата например имат напълно пълни външни черупки и рядко участват в химични реакции.
Елементите обикновено се класифицират като метални или неметални, но разделителната линия между двете е размита. Металните елементи обикновено са добри проводници на електричество и топлина. Подгрупите в металите се основават на сходните характеристики и химичните свойства на тези колекции. Нашето описание на периодичната таблица използва общоприети групи от елементи, според Националната лаборатория в Лос Аламос.
Алкални метали: Алкалните метали съставляват по-голямата част от група 1, първата колона на таблицата. Достатъчно лъскави и меки, за да се нарязват с нож, тези метали започват с литий (Li) и завършват с франций (Fr). Те също са изключително реактивни и ще избухнат в пламък или дори ще избухнат при контакт с вода, така че химиците ги съхраняват в масла или инертни газове. Водородът със своя единичен електрон също живее в група 1, но газът се счита за неметал.
Алкалоземни метали: Алкалоземните метали съставят група 2 на периодичната таблица, от берилий (Be) до радий (Ra). Всеки от тези елементи има два електрона в най-външното си енергийно ниво, което прави алкалните земи достатъчно реактивни, че рядко се срещат сами в природата. Но те не са толкова реактивни, колкото алкалните метали. Техните химични реакции обикновено протичат по-бавно и произвеждат по-малко топлина в сравнение с алкалните метали.
Лантанидите: Третата група е много прекалено дълга, за да се впише в третата колона, така че тя се разбива и се премества настрани, за да се превърне в горния ред на острова, който плува в дъното на таблицата. Това са лантанидите, елементи от 57 до 71 - лантан (La) до лютеций (Lu). Елементите от тази група имат сребристо бял цвят и оцветяват при контакт с въздух.
актинидите: Актинидите изравняват долния ред на острова и съдържат елементи 89, актиний (Ac), до 103, Lawrencium (Lr). От тези елементи само торий (Th) и уран (U) се срещат естествено на Земята в значителни количества. Всички са радиоактивни. Актинидите и лантанидите заедно образуват група, наречена вътрешни преходни метали.
Преходни метали: Връщайки се към основното тяло на таблицата, останалите групи от 3 до 12 представляват останалите преходни метали. Твърди, но податливи, лъскави и притежаващи добра проводимост, тези елементи са онова, за което обикновено се сещате, когато чуете думата метал. Тук живеят много от най-големите хитове на света на металите - включително злато, сребро, желязо и платина.
Следпреходни метали: Преди скока в неметалния свят споделените характеристики не са добре разделени по вертикални групови линии. След преходните метали са алуминий (Al), галий (Ga), индий (In), талий (Tl), калай (Sn), олово (Pb) и бисмут (Bi) и те обхващат група 13 до група 17. Тези елементи имат някои от класическите характеристики на преходните метали, но те са склонни да бъдат по-меки и да действат по-лошо от другите преходни метали. Много периодични таблици ще съдържат удебелена "стълбищна" линия под диагонала, свързващ бор с астатин. Металите след прехода се струпват в долната лява част на тази линия.
металоиди: Металоидите са бор (В), силиций (Si), германий (Ge), арсен (As), антимон (Sb), телур (Te) и полоний (Po). Те образуват стълбището, което представлява постепенния преход от метали към неметали. Тези елементи понякога се държат като полупроводници (B, Si, Ge), а не като проводници. Металоидите също се наричат "полуметали" или "лоши метали".
неметали: Всичко останало в горния десен ъгъл на стълбището - плюс водород (Н), върнат обратно в група 1 - е неметал. Те включват въглерод (С), азот (N), фосфор (P), кислород (O), сяра (S) и селен (Se).
Халогени: Четирите най-важни елемента от група 17, от флуор (F) до астатин (At), представляват един от двата подмножества на неметалите. Халогените са доста химически реактивни и са склонни да се свързват с алкални метали, за да произвеждат различни видове сол. Солта за трапеза във вашата кухня например е брак между натрия на алкален метал и халогенния хлор.
Благородни газове: Безцветни, без мирис и почти напълно нереактивни, инертните или благородни газове закръглят масата в група 18. Много химици очакват оганессон, един от четирите новоименувани елемента, да споделят тези характеристики; обаче, тъй като този елемент има измерване на полуживот в милисекунди, никой не е успял да го тества директно. Oganesson завършва седмия период на периодичната таблица, така че ако някой успее да синтезира елемент 119 (и състезанието да го направи вече е в ход), той ще се върти около, за да започне ред осми в колоната на алкален метал.
Поради цикличния характер, създаден от периодичността, която дава на таблицата името, някои химици предпочитат да визуализират таблицата на Менделеев като кръг.
Допълнителен ресурси: