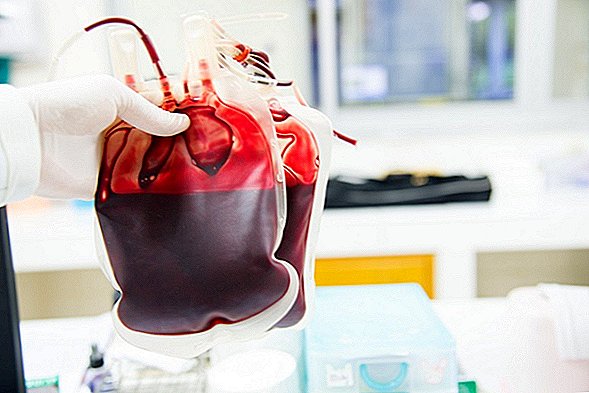
Ако смятате, че идеята за получаване на трансфузия с "млада кръв", за да се предотврати стареенето, звучи нагледно, добре, американските здравни служители са съгласни.
Днес (19 февруари) Американската агенция по храните и лекарствата (FDA) заяви, че е обезпокоена от доклади на „лоши актьори“, предлагащи вливания на кръвна плазма от млади хора, за уж лечение на състояния и заболявания, свързани с възрастта, такава загуба на паметта, Болест на Паркинсон и Алцхаймер. Такива лечения са не само недоказани, но и носят потенциално сериозни рискове, посочват от агенцията.
„Най-просто казано, притеснени сме, че някои пациенти биват преследвани от безскрупулни актьори, които изказват лечението на плазмата от млади донори като лекове и лекарства“, д-р Скот Готлиб, комисар на FDA, и д-р Питър Маркс, директор на FDA Център за биологична оценка и изследвания, се казва в изявление. „Такива лечения нямат доказани клинични ползи за употребите, за които тези клиники ги рекламират и са потенциално вредни.“
Плазмата е течната част от кръвта и не съдържа кръвни клетки. Преливане с плазма може да бъде животоспасяващо за хора, които преживяват физическа травма или имат определени заболявания или състояния, които не позволяват на кръвта им да се съсирва правилно.
Но FDA не е одобрила плазмени трансфузии за лечение на свързани с възрастта състояния и заболявания и не се знае, че тези лечения са безопасни или ефективни.
„Силно възпрепятстваме потребителите да прилагат тази терапия извън клинични изпитвания“, които са получили подходящ преглед и регулаторен надзор, заявиха Готлиб и Маркс.
Нещо повече, някои доклади сочат, че тези неодобрени трансфузии могат да включват големи обеми плазма и такива големи дози са свързани със "значителни рискове", като инфекции, алергични реакции и проблеми с дишането и сърдечно-съдовата система, се казва в изявлението.
FDA призова потребителите да се консултират с лекарите си, преди да обмислят подобно лечение. В допълнение, клиничните изпитвания, които тестват кръвопреливане за цели, които все още не са одобрени от FDA, трябва да имат "разследващо приложение на ново лекарство (IND) с FDA, което означава, че агенцията е прегледала експерименталната терапия, за да се увери, че тя е безопасна , Така че, ако се каже, че терапията за кръвопреливане се предлага като част от клинично изпитване, хората трябва да поискат да видят IND номера и копие от съобщението на FDA, потвърждаващо заявлението, посочва агенцията.